作者:
Randy Alexander
创建日期:
2 四月 2021
更新日期:
1 七月 2024

内容
化学方程式是化学反应的符号表示。试剂写在左侧,产品写在右侧。质量守恒定律表明在化学反应中没有原子生或丢失,因此反应物中存在的原子数必须等于反应中存在的原子数。产品。遵循本教程,您可以用不同的方式平衡化学方程式。
脚步
方法1之2:按照传统方法进行平衡
写下给定的方程式。 在此示例中,您将具有: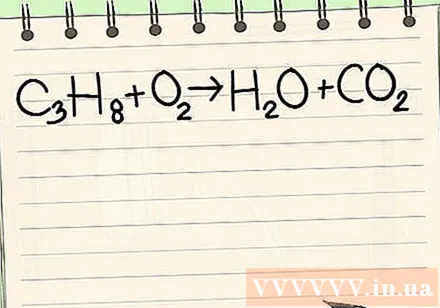
- C3H8 + O2 ->高2氧气+一氧化碳2
- 当丙烷(C3H8在氧气中燃烧生成水和二氧化碳。

写下等式两边各元素的原子数。 请参阅每个原子旁边的下面的索引,以找到方程中的原子数。- 左:3个碳,8个氢和2个氧。
- 右:1个碳,2个氢和3个氧。
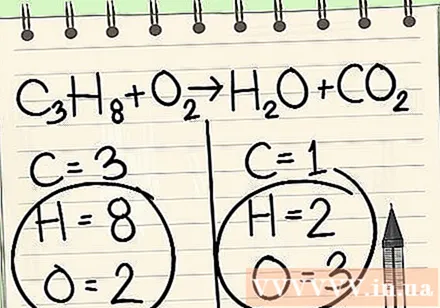
最终要始终保留氢气和氧气。
如果您还有多个要素需要平衡: 选择仅出现在反应物的单个分子中且仅出现在产物的单个分子中的元素。这意味着您将需要首先平衡碳原子。
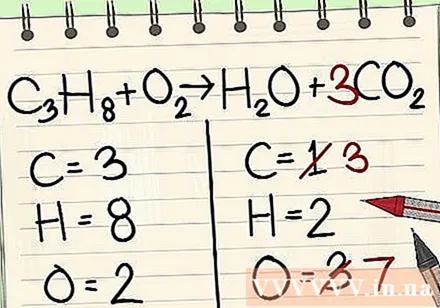
将单个碳原子的系数添加到方程式的右侧,以使其与方程式左侧的三个碳原子平衡。- C3H8 + O2 ->高2O + 3CO2
- 右侧碳前面的因子3表示存在3个碳原子,而左侧的sub-3表示3个碳原子。
- 在化学方程式中,您可以更改系数,但不能更改下标。
接下来是氢原子平衡。 您的左侧有8个氢原子。因此,您将需要在右侧8。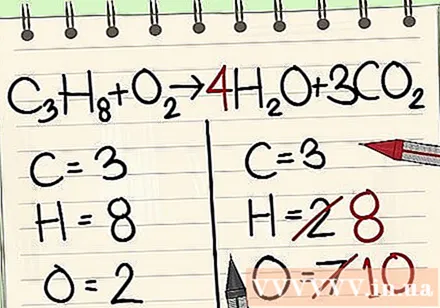
- C3H8 + O2 -> 4小时2O + 3CO2
- 在小时的右边,将4作为因子,因为底部数字显示您已经有2个氢原子。
- 将系数4乘以索引2时,得到8。
- 其他6个氧原子来自3CO2。(3x2 = 6个氧原子+ 4个其他氧原子= 10)
平衡氧原子。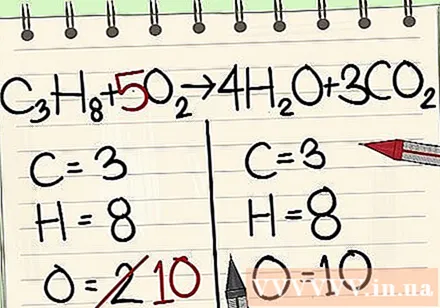
- 因为您已在方程式右边的分子中添加了系数,所以氧原子数已更改。现在您在水分子中有4个氧原子,在二氧化碳分子中有6个氧原子。我们总共有10个氧原子。
- 将因子5加到方程式左侧的氧分子中。现在每侧有10个氧分子。
- C3H8 + 5O2 -> 4小时2O + 3CO2.

- 碳,氢和氧原子处于平衡状态。您的方程式是完整的。
方法2之2:按照代数方法求平衡
根据符号和公式编写方程式。 示例a = 1并根据该公式编写方程。
用其变量替换数字。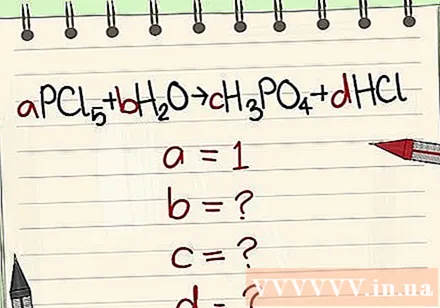
检查反应侧和产物侧的元素数量。
- 示例:aPCl5 + bH2O = cH3PO4 + dHCl,因此a = 1 b = c = d =并将元素P,Cl,H,O分离,因此得到a = 1 b = 4 c = 1 d = 5 。
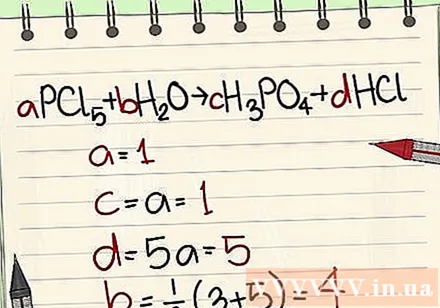
- 示例:aPCl5 + bH2O = cH3PO4 + dHCl,因此a = 1 b = c = d =并将元素P,Cl,H,O分离,因此得到a = 1 b = 4 c = 1 d = 5 。
忠告
- 记住要简化方程式。
- 如果遇到问题,可以在在线平衡工具中输入一个方程式来平衡它。请记住,参加考试时您无权使用在线余额,所以请不要依赖它。
警告
- 切勿在化学方程式中使用系数作为分数-在化学反应中不能除以分子或原子。
- 在平衡过程中,可以使用分数,但是如果系数仍然是分数,则方程将不会平衡。
- 要删除分数,请将整个方程(左右两边)乘以分数的分母。



