作者:
Helen Garcia
创建日期:
17 四月 2021
更新日期:
1 七月 2024

内容
当量度表示溶液中酸或碱的浓度。为了找出溶液的正态性,可以在计算中使用分子的摩尔浓度和当量质量。如果您选择使用摩尔浓度,请使用公式 N = M (n),其中 M 是摩尔浓度,n 是氢或氢氧化物分子的数量。如果您决定使用等效质量,请使用公式 N = eq ÷ V,其中 eq 是当量数,V 是溶液的体积。
脚步
方法 1 of 2:通过摩尔浓度计算正态性
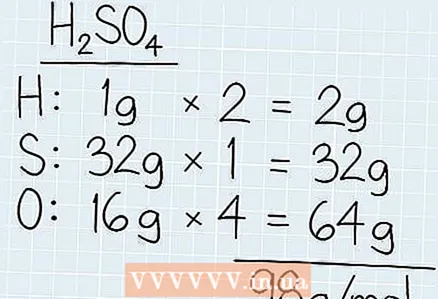 1 将溶液所有组分的摩尔质量相加。 找出元素周期表上化学式的元素,找出它们的原子质量,它对应于摩尔质量。写下每个元素的摩尔质量并将其乘以这些元素的数量。将所有组分的摩尔质量相加得到总摩尔质量。
1 将溶液所有组分的摩尔质量相加。 找出元素周期表上化学式的元素,找出它们的原子质量,它对应于摩尔质量。写下每个元素的摩尔质量并将其乘以这些元素的数量。将所有组分的摩尔质量相加得到总摩尔质量。 - 例如,如果您想知道硫酸的摩尔质量 (H2所以4),找出氢 (1 g)、硫 (3 g) 和氧 (16 g) 的摩尔质量。
- 将质量乘以组合物中的组分数。在我们的示例中,有 2 个氢原子和 4 个氧原子。氢的总摩尔质量为 2 x 1 g = 2 g。该溶液中氧的摩尔质量为 4 x 16 g = 64 g。
- 将所有摩尔质量加在一起。你得到 2 g + 32 g + 64 g = 98 g/mol。
- 如果您已经知道您正在寻找的溶液的摩尔浓度,请直接转到第 4 步。
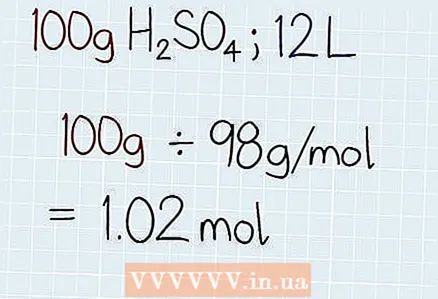 2 将溶液的实际质量除以摩尔质量。 找出溶液的实际重量。它将在带有解决方案的容器上或任务本身中指示。然后将溶液的质量除以之前发现的总摩尔质量。结果将是溶液中的摩尔数,其后应写上“摩尔”。
2 将溶液的实际质量除以摩尔质量。 找出溶液的实际重量。它将在带有解决方案的容器上或任务本身中指示。然后将溶液的质量除以之前发现的总摩尔质量。结果将是溶液中的摩尔数,其后应写上“摩尔”。 - 例如,如果您试图找出 100 g H 的正态性2所以4溶解在 12 升液体中,用实际质量除以摩尔数。结果,您将得到:100 g ÷ 98 g / mol = 1.02 mol。
- 1 摩尔等于溶液的 6.02 x 10 个原子或分子。
 3 将结果除以以升为单位的溶液体积以找出摩尔浓度。 将刚刚计算的溶液中的摩尔数除以待测溶液的总体积。结果,您将知道摩尔浓度 (M),通过它您可以找出溶液的浓度。
3 将结果除以以升为单位的溶液体积以找出摩尔浓度。 将刚刚计算的溶液中的摩尔数除以待测溶液的总体积。结果,您将知道摩尔浓度 (M),通过它您可以找出溶液的浓度。 - 根据我们的示例,我们得到以下公式:1.02 mol ÷ 12 L = 0.085 M。
建议: 如果您还没有这样做,请务必将溶液的体积转换为升。否则,您将得到错误的答案。
 4 将摩尔浓度乘以氢或氢氧化物分子的数量。 查看化学式,找出酸中氢原子 (H) 或碱中 (OH) 中的氢氧化物分子的数量。然后将溶液的摩尔浓度乘以该溶液中氢或氢氧化物分子的数量,以找到正常浓度或当量。在答案的末尾,写下缩写“N”。
4 将摩尔浓度乘以氢或氢氧化物分子的数量。 查看化学式,找出酸中氢原子 (H) 或碱中 (OH) 中的氢氧化物分子的数量。然后将溶液的摩尔浓度乘以该溶液中氢或氢氧化物分子的数量,以找到正常浓度或当量。在答案的末尾,写下缩写“N”。 - 在我们的例子中,硫酸(H2所以4) 2 个氢原子。所以公式将是这样的:0.085 M x 2 = 0.17 N。
- 在另一个例子中,摩尔浓度为2M的氢氧化钠(NaOH)只有1个氢氧化物分子。因此,公式如下:2 M x 1 = 2 N。
方法 2 of 2:计算等效质量的正态性
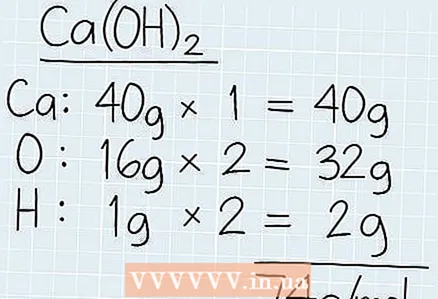 1 找出溶液的总摩尔质量。 看一看溶液的化学式,找出元素周期表上的每个元素。写下每种元素的摩尔质量,然后乘以公式中这些元素的数量。将所有摩尔质量加在一起以找到以克为单位的总摩尔质量。
1 找出溶液的总摩尔质量。 看一看溶液的化学式,找出元素周期表上的每个元素。写下每种元素的摩尔质量,然后乘以公式中这些元素的数量。将所有摩尔质量加在一起以找到以克为单位的总摩尔质量。 - 例如,如果您想知道 Ca (OH) 的摩尔质量2,然后找出钙 (40 g)、氧 (16 g) 和氢 (1 g) 的摩尔质量。
- 式中有2个氧原子和氢原子。氧气的总质量为:2 x 16 g = 32 g。氢气的摩尔质量为:2 x 1 g = 2 g。
- 将所有摩尔质量加在一起得到 40 g + 32 g + 2 g = 74 g/mol。
 2 将摩尔质量除以氢或氢氧化物分子的数量。 找出碱中酸或氢氧化物 (OH) 分子中的氢原子 (H) 数。将刚刚得到的总摩尔质量除以原子或分子的数量,找出 1 当量的重量,这将等于 1 摩尔氢或氢氧化物的质量。在答案的末尾,写上缩写“G.-e.”,意思是等价物的质量。
2 将摩尔质量除以氢或氢氧化物分子的数量。 找出碱中酸或氢氧化物 (OH) 分子中的氢原子 (H) 数。将刚刚得到的总摩尔质量除以原子或分子的数量,找出 1 当量的重量,这将等于 1 摩尔氢或氢氧化物的质量。在答案的末尾,写上缩写“G.-e.”,意思是等价物的质量。 - 在我们的例子中,Ca (OH)2 2 两个氢分子,这意味着当量的质量将等于 74 g/mol ÷ 2 = 37 G.-e。
 3 将溶液的实际重量除以当量重量。 知道等价物的质量后,将其除以溶液的质量,该质量在装有溶液的容器或正在解决的问题中标明。答案将是解中等价物的数量,以便您可以计算正态性。在答案的末尾,加上缩写“e”。
3 将溶液的实际重量除以当量重量。 知道等价物的质量后,将其除以溶液的质量,该质量在装有溶液的容器或正在解决的问题中标明。答案将是解中等价物的数量,以便您可以计算正态性。在答案的末尾,加上缩写“e”。 - 如果在我们的示例中 75 g Ca (OH)2,则公式如下:75 g ÷ 37 G.-e = 2.027 Oe。
 4 将当量数除以以升为单位的溶液体积。 找出溶液的总体积并以升为单位写下答案。取刚刚得到的等价数除以解的体积,找出正态性。在你的答案末尾加上一个缩写“N”。
4 将当量数除以以升为单位的溶液体积。 找出溶液的总体积并以升为单位写下答案。取刚刚得到的等价数除以解的体积,找出正态性。在你的答案末尾加上一个缩写“N”。 - 如果体积为 8 升的溶液中有 75 克 Ca (OH)2,然后按以下方式将当量数除以体积:2.027 Oe。 ÷ 8 l = 0.253 N。
提示
- 正常浓度或正态性通常用于测量酸和碱。如果您需要确定另一种溶液的浓度,通常通过测量摩尔浓度来完成。
你需要什么
- 元素周期表
- 计算器