作者:
Lewis Jackson
创建日期:
6 可能 2021
更新日期:
1 七月 2024

内容
平均质量原子不是原子质量的直接量度。相反,这是元素典型样品中每个原子的平均质量。如果您可以测量数十亿个单个原子的质量,则可以通过计算它们的平均值来找出它们。我们有一个更实用的方法,该方法基于有关化学元素不同同位素的信息。
脚步
第1部分,共2部分:计算平均质量原子
了解同位素和质量原子。 在自然界中,大多数元素都以多种形式或同位素存在。同一元素的两个同位素之间唯一的区别是原子中的中子数,中子数影响质量原子。计算原子的平均质量时会考虑到这种差异的影响,并告诉您这些原子的样本中每个原子的平均质量。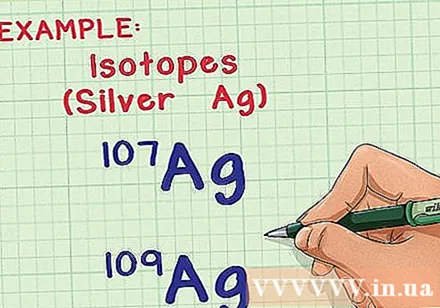
- 例如,元素银(Ag)具有两种天然同位素:Ag-107和Ag-109(或Ag和Ag)。同位素以“质量数”或原子中质子数和中子数的总和来命名。这意味着Ag-109的中子比Ag-107多两个,因此它的原子重一些。
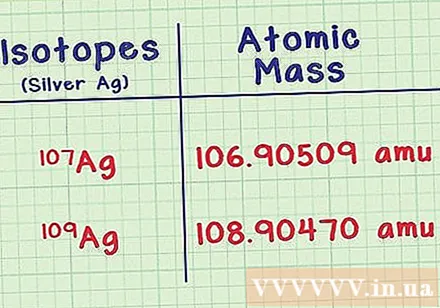
找到每种同位素的质量。 每个同位素都需要两条信息,您可以在参考书中查找它们,也可以在线查找,例如webelements.com。第一个是每个同位素的质量原子或原子质量。具有更多中子的同位素具有更大的质量。- 例如,银同位素Ag-107具有质量原子 106,90509 amu (立方原子的单位)。同位素Ag-109的质量略重 108,90470.
- 文件末尾的小数点对可能略有不同。质量后不要在括号内写任何数字。

写下每种同位素的自然存活率。 该速率表示同位素的流行程度,以元素总原子的百分比表示。您可以在同一文档中找到带有立方原子的信息。所有同位素的自然存活率应为100%(尽管由于四舍五入的误差可能会略有差异)。- Ag-107同位素的比例为51.86%。同位素Ag-109较少见,比率为48.14%。这意味着正常的银样品具有51.86%的Ag-107和48.14%的Ag-109。
- 没有此存活率的任何同位素都将被忽略。这些同位素在地球上并不自然存在。

将同位素百分比转换为十进制数。 将该比率除以100将得到与小数相同的值。- 在上面的银样品中,同位素比为51.86 / 100 = 0,5186 和48,14 / 100 = 0,4814.
找到平均立方原子。 元素的平均质量原子具有 ñ 同位素相等 (原子块同位素1 *比率同位素1)+(原子质量同位素2 *比率同位素2)+ ... +(原子质量同位素 ñ *比率同位素 ñ。这是“平均质量”的一个例子,这意味着同位素的存活率越大,其对结果的影响就越大。对于银,如何应用此公式如下:
- 中等质量原子银 =(立方原子银107 *比率银107)+(原子质量银109 *比率银109)
=(106,90509 * 0,5186) + (108,90470 * 0,4814)
= 55,4410 + 52,4267
= 107.8677 amu。 - 在元素周期表中找到该元素以检查结果。平均立方原子始终写在元素的化学符号下方。
- 中等质量原子银 =(立方原子银107 *比率银107)+(原子质量银109 *比率银109)
第2部分(共2部分):使用结果
将质量转换为原子序数。 平均质量原子表示该元素的典型样品中质量与原子数之间的关系。这在化学实验室中非常有用,因为几乎不可能精确地计数原子,但是质量很容易确定。例如,您可以称重一个银样品,并知道每107,8677 amu将有一个银原子。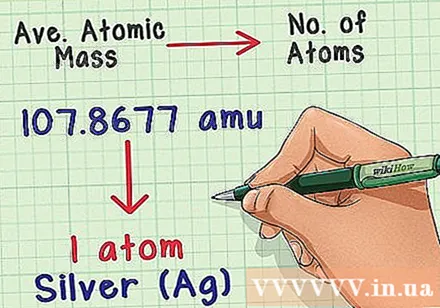
转换为摩尔质量. 原子质量单位非常小,因此化学家经常使用克单位质量。幸运的是,我们已经定义了这些概念,因此转换应该很容易。只需将平均质量原子乘以1 g / mol(摩尔质量常数)即可得到g / mol的结果。例如,107,8677克的银包含一摩尔的银原子。
求出平均分子量。 由于分子是原子的集合,因此您可以将所有原子的质量相加即可找到分子质量。如果使用平均质量原子(而不是特定同位素的质量),则结果将是自然界中样品的平均分子量。这是一个例子: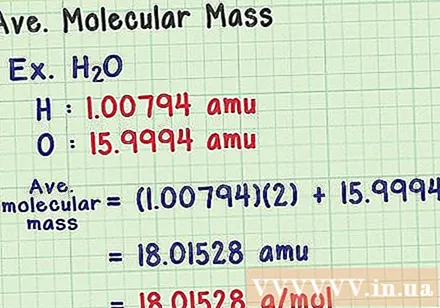
- 水分子的化学式为H2O包含两个氢原子(H)和一个氧(O)原子。
- 氢的平均质量原子为1,00794 amu。氧气的平均原子质量为15,9994 amu。
- 所以H的平均分子量2O等于(1,00794)(2)+ 15,9994 = 18,01528 amu,相当于18,01528 g / mol。
忠告
- 相对原子质量的概念有时与平均质量原子同义使用。由于原子质量相对单位不大,因此存在细微差别。它是相对于碳12原子的质量的量度。只要在平均立方原子计算中使用原子质量单位,这两个值是相同的。
- 立方原子后面括号中的数字告诉我们该错误。例如,质量原子1.0173(4)表示元素的普通原子的质量范围约为1.0173±0.0004。如果不需要,则无需获取此号码。
- 在元素周期表上,除少数例外,随后元素的平均立方原子大于之前的原子。这是检查结果的快速方法。
- 1原子质量单位是碳12原子的质量的1/12。
- 同位素存活率是根据地球上自然产生的典型样本计算得出的。非天然存在的物质,例如陨石或实验室生产的一种物质,可能具有不同的同位素比,因此平均质量原子也不同。
警告
- 质量原子始终以原子质量单位(amu或u)书写,有时也称为道尔顿(Da)。请勿在未更改此数字后再写其他质量单位(例如千克)。
你需要什么
- 铅笔
- 纸
- 笔记本电脑
- 自然界中同位素存活率的数据。
- 同位素的质量原子单位数据。